In kontrollierten klinischen Studien treten immer wieder Studienabbrecher oder Protokollverletzungen auf. Nach den GCP Richtlinien werden dazu verschiedene Studienpopulationen definiert. Intention-To-Treat Population stellt dabei eine wichtige Auswertepopulation dar (ITT Analysis). According-To-Protocol (ATP) oder Per-Protocol (PP) Gesamtheiten stellen dagegen sehr saubere Populationen dar, die die reinen Behandlungseffekte widerspiegeln. In diesem Artikel zeigen wir, welche Populationen im Anwendungsbereich medizinische Statistik bei der Auswertung kontrollierter klinischer Studien unterschieden werden. Dabei grenzt man die unterschiedlichen Gesamtheiten hinsichtlich ihrer Aussagen voneinander ab.
Wenn Sie Unterstützung bei der Planung oder Auswertung klinischer Studien benötigen, können Ihnen unsere sachkundigen Statistiker jederzeit weiterhelfen. Kontaktieren Sie uns für ein unverbindliches Angebot!
Diese Artikel beantwortet folgende Fragen:
- In welche Abschnitte unterteilt sich eine klinische Studie?
- Warum muss man verschiedene Auswertepopulationen für die medizinische Statistik berücksichtigen?
- Was versteht man unter Intention-To-Treat, According-To-Protocol, Per-Protocol?
- Gibt es noch andere Auswertepopulationen?
- Was muss bei der ITT Analysis beachtet werden?
Die kontrollierte klinische Studie – der lange Weg zur Überprüfung der Wirksamkeit
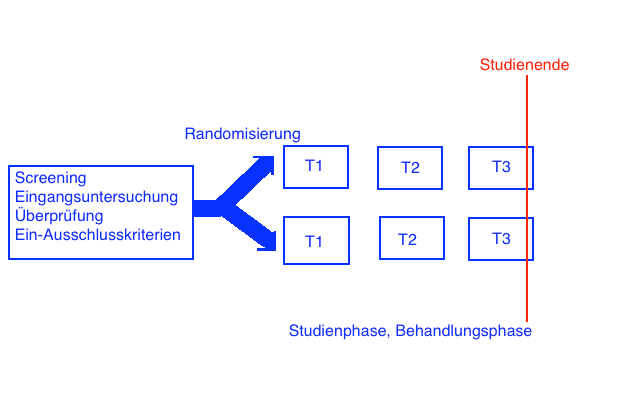
Kontrollierte klinische Studien werden meist über einen längeren Zeitraum hinweg durchgeführt. Nach der Rekrutierungsphase und der Überprüfung der Einschluss- und Ausschlussbedingungen werden Patienten den jeweiligen Behandlungsästen zugeordnet. Erfolgt die Zuweisung zufällig, so spricht man von Randomisierung. Anschliessend erfolgt die Studienphase, in der meist in mehreren Abschnitten verschiedene Untersuchungen durchgeführt werden und Werte erhoben werden. In der Studienphase werden unter strenger ärztlicher Kontrolle die Behandlungen oder Interventionen wie im Studienprotokoll vorgesehen durchgeführt. Am Ende dieser Phase erfolgt die Abschlussuntersuchung und damit das Ende der Behandlung. Mitunter schliessen sich noch mehrere Follow-Up Zeitpunkte an, in denen der weitere Verlauf nach Studienabschluss nach vorher definierten Schemata erhoben wird. So kann man Langzeiteffekte und zeitverzögerte Folgen untersuchen und beurteilen.
Sie haben Fragen rund um den Themenkomplex klinische Studien, zum Studienprotokoll, zur Studienplanung oder Auswertung klinischer Studien? Unseren Experten stehen für professionelle Unterstützung für klinische Studien jederzeit zur Verfügung. Wir helfen Ihnen auch bei komplexen Designs und Auswertungen weiter. Nehmen Sie Kontakt mit uns auf!
Missing Values, Protokollverletzer und Dropout: das Problem mit unvollständigen Daten
Bei Verlaufs- oder Beobachtungsstudien, bei denen Patienten über einen längeren Beobachtungszeitraum therapiert bzw. beobachtet werden, ist die Wahrscheinlichkeit unvollständiger Datensätze erhöht. Im Studienverlauf werden meist wiederholt Messungen der interessierenden Zielvariablen vorgenommen. Die Ursachen für fehlende Werte (missing values) sind dabei vielfältig: Zum Teil stehen die Studienteilnehmer absichtlich oder unabsichtlich nicht für die Erfassung der Daten zur Verfügung, sei es wegen Krankheit, Reise, beruflicher Verpflichtung oder anderen Gründen. Es kann vorkommen, dass aufgrund technischer Probleme Messungen nicht korrekt vorgenommen werden können.
Davon unabhängig können und müssen noch andere Schwierigkeiten berücksichtigt werden. Als Protokollverletzer bezeichnet man Studienteilnehmer, die einem Behandlungsarm zugewiesen wurden, sich aber nicht an die vorgeschriebene Therapie halten. Dabei können beispielsweise zusätzliche Medikamente eingenommen werden, die Behandlung nicht im vorgesehenen Zeitfenster durchgeführt werden oder die Einnahme vergessen oder verweigert werden. Auch hier gibt es viele verschiedene Varianten. Solche Patienten sollte man nach Möglichkeit weiter beobachten und man sollte versuchen, ein weiteres Einhalten des Therapieschemas zu ermöglichen. Jede Therapieverletzung wird sorgfältig dokumentiert.
Es kann aber auch sein, dass Studienteilnehmer nach der Randomisierung aus der Studie ausscheiden wollen oder müssen. So kann durch einen Umzug der Weg zum Studienarzt zu umständlich werden oder eine Schwangerschaft kann den Studienabbruch erfordern. Grundsätzlich haben alle Studienteilnehmer das Recht, ohne Angabe von Gründen jederzeit die Teilnahme abzubrechen. Studienabbrecher bezeichnet man auch als Drop-out.
Folgen unvollständiger Datensätze: Ignorieren geht nicht!
Je länger eine prospektive Studie dauert, umso höher ist die Wahrscheinlichkeit unvollständiger Datensätze, sei es durch Missing Values, Drop-out oder Protokollverletzer. Als problematisch erweisen sich diese unvollständigen Datensätze bei der Auswertung der Daten. Wenn man für die Analysen standardmässig nur Daten von Studienteilnehmer verwendet, die alle Messungen nach Protokoll absolviert haben, führt dies zwangsläufig zu einer z. T. erheblichen Reduktion der Fallzahl und damit einem enormen Powerverlust. Medizinisch relevante Unterschiede können durch medizinische Statistik nicht mehr nachgewiesen werden. Gleichzeitig muss ausgeschlossen werden, dass mögliche systematische Ursachen hinter dem Fehlen stecken. Ist ein Behandlungsarm stärker von fehlenden Werten betroffen? Auf diese Weise muss eine Verzerrung (Bias) der Studienergebnisse ausgeschlossen werden.
Verzerrung durch fehlende Werte
Ein Ausschluss unvollständiger Datensätze bringt aber nicht nur einen zum Teil erheblichen Powerverlust mit sich, sondern bereinigt die Daten auch noch. Studienteilnehmer, die im Laufe der Studie Unregelmässigkeiten zeigten, sind so von der Auswertung und der Überprüfung der Wirksamkeit ausgeschlossen. Solche idealen aber unrealistischen Szenarien sind für viele Fragestellungen gar nicht erwünscht oder geeignet. Aus diesem Grund führt man Auswertungen klinischer Studien an verschiedenen Studienpopulationen durch.
Intention-To-Treat vs. According-To-Protocol: Die verschiedenen Studienpopulation
Abhängig von der Art der Auswertung berücksichtigt man für die medizinische Statistik verschiedenen Auswertepopulationen. Die wichtigsten Populationen dabei sind:
Intention-to-treat Population
Die Intention-To-Treat (ITT) Analysis ist eine Auswertestrategie entsprechend den Regeln der sogenannten Good Clinical Practice (GCP). Sie ist damit bindend für zulassungsrelevante klinische Studien und wird als Goldstandard in der Auswertung betrachtet. Die ITT Analysis sieht vor, alle Studienteilnehmer entsprechend der zugewiesenen (randomisierten) Behandlungsgruppe auszuwerten, und zwar unabhängig davon, was nach diesem Zeitpunkt der Gruppenzuteilung geschieht. Man wertet alle Studienteilnehmer entsprechend der Behandlungsgruppe aus, zu der sie initial (bei Randomisierung) zugeteilt wurden, auch wenn diese im weiteren Verlauf beispielsweise die Behandlung wechseln oder ganz aus der Studie ausscheiden.
According-To-Protocol Population
Die According-To-Protocol Population (ATP) oder auch Per-Protocol Population (PP) dagegen umfasst alle Studienteilnehmer, die sich im Studienverlauf bzw. bis zu einem festgelegten Studienabschnitt gemäss des Studienprotokolls verhalten haben. Protokollverletzer werden bei dieser Art der Auswertung ausgeschlossen und nicht berücksichtigt. Welche Protokollverletzungen dabei konkret ausgeschlossen werden, muss im Studienprotokoll klar definiert sein. Wenn man ausschliesslich eine Per-Protocol Analysis durchführt, so führt dies zu einer Verzerrung der Ergebnisse: Die Wirksamkeit der Behandlungen wird durch den Ausschluss von Protokollverletzer höher geschätzt, als in der Realität zu erwarten ist. Daher wird eine ATP Auswertung immer ergänzend zur ITT Analysis durchgeführt.
As-Treated (AT)
Als dritte, weniger häufig anzutreffende Auswertestrategie gilt der As-Treated (AT) Ansatz. Hier analysiert man die Patienten in den tatsächlich durchgeführten Behandlungsgruppen. Die Zuordnung zum Zeitpunkt der Randomisierung spielt dabei im Gegensatz zu ITT Analyse und PP Analyse keine Rolle. Diese Art der Auswertung findet nur selten Anwendung, zumeist bei dem Vergleich operativer und medikamentöser Behandlungen.
Weitere Populationen
Darüberhinaus gibt es noch
Safety Analysis Set (SAF): Diese Population enthält alle Studienteilnehmer, die randomisiert wurden und mindestens eine Behandlung erhalten haben.
Full-Analysis-Set (FAS): Diese Population umfasst alle Studienteilnehmer des SAF, für die zusätzlich mindestens ein Wirksamkeitsmass des primären Endpunktes nach der ersten Behandlung vorliegt.
Zusammenfassung: Mit fehlenden Daten umgehen durch Intention-To-Treat Prinzip
Die medizinische Statistik ist geprägt von vielen regulatorischen Vorgaben, die eine korrekte Schlussfolgerung auf Basis der Studienergebnisse erlauben soll.
Bei der Auswertung klinischer Studien existieren sehr viele regulatorische Vorgaben, die man bereits in der Planungsphase berücksichtigen muss. Die Festlegung der Auswertepopulationen stellt dabei einen wichtigen Aspekt dar. So müssen beispielsweise Analysen nach dem Intention-To-Treat Prinzip (ITT Analysis) durchgeführt werden. Für die Arzneimittelsicherheit und die Untersuchung von unerwünschten Nebenwirkungen sind dagegen andere Auswertepopulationen (SAF) relevant.
Bei Fragen zu regulatorischen Aspekten sowie Hilfestellungen zur Studienplanung, dem Erstellen von Studienprotokollen oder der Auswertung klinischer Studien stehen unsere Biometriker und unsere Studienexperten mit Rat und Tat zur Seite. Nehmen Sie Kontakt mit uns auf, und schildern Sie uns Ihre Herausforderung. Unsere Studienexperten helfen Ihnen dabei gerne. Wir freuen uns auf Sie!
Weiterführende Literatur zur Intention-To-Treat Analyse
Martin Schumacher, Gabi Schulgen – Methodik klinischer Studien: Methodische Grundlagen der Planung, Durchführung und Auswertung. 3. Auflage
