Der Begriff Proof of Concept (PoC) bezeichnet ein grundlegendes Prinzip in Entwicklungsprozessen. Es wird häufig auch als Machbarkeitsstudie bezeichnet und prüft, ob ein Konzept oder Wirkprinzip unter realistischen Bedingungen grundsätzlich funktioniert. Ziel ist es, frühzeitig eine belastbare Entscheidungsgrundlage zu schaffen, bevor weiterführende Schritte erfolgen.
Im medizinischen Kontext erhält der PoC eine spezifische Bedeutung. Er zielt darauf ab zu zeigen, dass ein medizinisches Wirkprinzip oder Konzept beim Menschen wirksam ist und geht damit über einen reinen Machbarkeitsnachweis hinaus. Entsprechend fungiert der PoC in der Medizin als zentraler Entscheidungspunkt innerhalb der klinischen Entwicklung unter Berücksichtigung von Sicherheit, ethischer Verantwortung und regulatorischem Rahmen.
Dieser Blogartikel erläutert zunächst die allgemeine Logik und Zielsetzung eines PoC. Anschließend ordnet er den PoC im medizinischen Entwicklungsprozess ein, beschreibt seine Rolle in unterschiedlichen medizinischen Anwendungsfeldern und grenzt ihn klar von vorgelagerten und nachgelagerten Studienphasen ab. Zuletzt wird dargestellt, welche Aussagekraft ein PoC besitzt und wo seine Grenzen liegen.
Proof of Concept in der Medizin: Zielsetzung und Aussagekraft
Ein PoC dient in der Medizin dazu, frühzeitig zu prüfen, ob ein medizinisches Konzept oder Wirkprinzip beim Menschen grundsätzlich trägt. Dazu wird eine klar definierte Annahme erstmals unter klinischen Bedingungen überprüft. Ziel ist es festzustellen, ob sich ein medizinisch relevanter Effekt nachweisen lässt und damit eine tragfähige Grundlage für die weitere Entwicklung besteht.
Zur Veranschaulichung lässt sich dies an einem typischen Beispiel festmachen. In der Arzneimittelentwicklung kann ein PoC zeigen, dass ein neuer Wirkstoff den erwarteten biologischen Effekt beim Menschen auslöst, etwa indem sich ein zuvor definierter Biomarker in die prognostizierte Richtung verändert. Ein solcher Befund liefert ein erstes Signal dafür, dass der zugrunde liegende Wirkmechanismus auch unter klinischen Bedingungen relevant ist.
Diese Prüfung erfolgt bewusst fokussiert. Der PoC richtet sich auf eine eng gefasste Fragestellung und verzichtet auf eine umfassende Bewertung des Ansatzes. Obwohl dabei eine konkrete Hypothese geprüft wird, ist die statistische Auswertung in der Regel nicht konfirmatorisch angelegt. Vielmehr dient sie der Bewertung eines frühen Signals und der Abschätzung von Effektgröße und Richtung, ohne bereits formale Wirksamkeitsnachweise zu erbringen.
Entsprechend ist die Aussagekraft eines PoC klar begrenzt. Ein positiver Befund bedeutet weder einen abschließenden Wirksamkeitsnachweis noch eine belastbare Aussage zur optimalen Anwendung. Fragen zur Dosiswahl, zur Langzeitsicherheit oder zur Übertragbarkeit auf größere Patientengruppen bleiben bewusst offen und werden in nachgelagerten Entwicklungsphasen adressiert.
Gerade diese klare Begrenzung macht den PoC zu einem wichtigen Entscheidungspunkt in der medizinischen Entwicklung. Er erlaubt es, frühzeitig zu beurteilen, ob die zugrunde liegende Idee ausreichend Substanz besitzt, um weitere Ressourcen zu rechtfertigen, oder ob ein Ansatz an dieser Stelle beendet werden sollte.
Einordnung des Proof of Concept im klinischen Entwicklungsprozess
Der PoC ist fest in den klinischen Entwicklungsprozess eingebettet. Seine Rolle wird insbesondere durch die Abgrenzung zu vor- und nachgelagerten Studienphasen deutlich. Während frühe klinische Studien vor allem Sicherheits- und Dosisfragen klären, dient der PoC dazu, erstmals einen medizinisch relevanten Effekt beim Menschen nachzuweisen. Erst durch diese Einordnung wird deutlich, welche Fragen ein PoC beantwortet und welche bewusst offenbleiben.
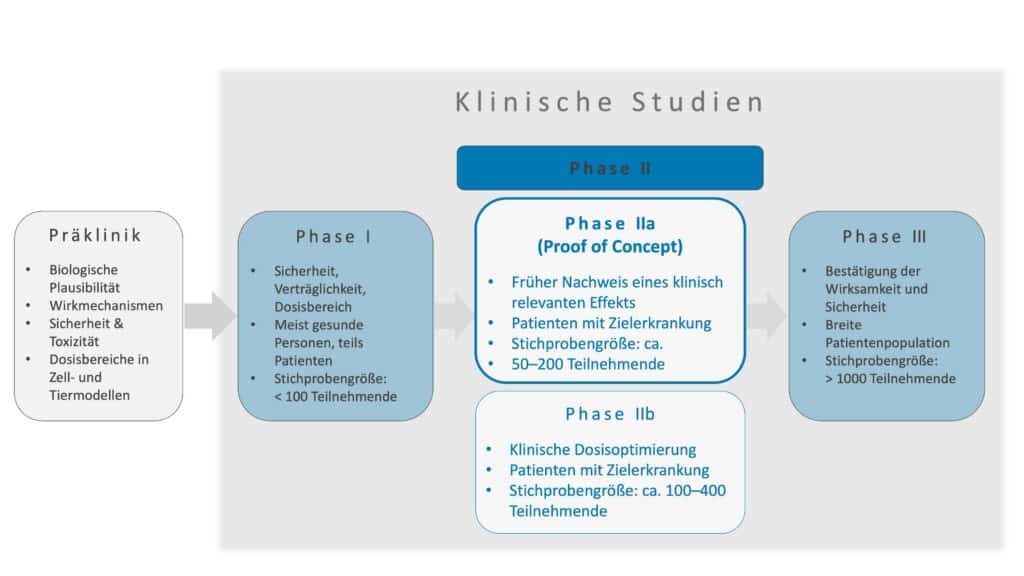
In frühen klinischen Studien steht zunächst die Sicherheit im Vordergrund. Phase-I-Studien klären Sicherheit und Verträglichkeit, häufig in Verbindung mit ersten Dosisinformationen. Sie dienen zudem der Charakterisierung pharmakokinetischer und pharmakodynamischer Zusammenhänge, nicht jedoch dem Nachweis klinischer Wirksamkeit.
Darauf aufbauend wird geprüft, ob das zugrunde liegende Wirkprinzip beim Menschen tatsächlich einen medizinisch relevanten Effekt entfaltet. Diese Fragestellung bezeichnet den PoC. Er stellt keine eigenständige klinische Phase dar, sondern beschreibt das inhaltliche Ziel, einen frühen Wirksamkeitsnachweis zu erbringen.
In der Literatur wird der Begriff nicht einheitlich verwendet. Während er in manchen Quellen bereits für sehr frühe Studien wie Phase-0- oder First-in-Human-Untersuchungen genutzt wird, bezieht er sich im klinischen Entwicklungsverständnis meist auf den ersten medizinisch relevanten Wirksamkeitsnachweis bei Patientinnen und Patienten. Hier wird der Begriff im Sinne eines klinischen PoC verstanden, der typischerweise im Rahmen von Phase-IIa-Studien erfolgt. Während Phase IIa den formalen zeitlichen Abschnitt der klinischen Entwicklung beschreibt, benennt der PoC die zentrale Fragestellung, die in diesem Abschnitt beantwortet werden soll.
Erst nach einem erfolgreichen PoC folgt eine systematische Dosisoptimierung, häufig im Rahmen von Phase IIb. In dieser Phase werden mehrere wirksame Dosen miteinander verglichen, um das Nutzen-Risiko-Profil für zulassungsrelevante Phase-III-Studien festzulegen. Diese Fragestellung geht bewusst über das hinaus, was ein PoC leisten soll.
In dieser Abfolge nimmt der PoC eine vermittelnde Rolle ein. Er verbindet frühe Sicherheits- und Dosisinformationen mit der späteren klinischen Optimierung und bildet damit einen zentralen Entscheidungspunkt im Entwicklungsprozess.
In welchen medizinischen Bereichen spielt Proof of Concept eine Rolle?
Der PoC wird im medizinischen Kontext in unterschiedlichen Anwendungsbereichen eingesetzt. Unabhängig vom konkreten Feld bleibt seine Funktion gleich, nämlich frühzeitig zu prüfen, ob ein medizinischer Ansatz einen relevanten Effekt zeigt. Die konkrete Ausgestaltung des PoC variiert jedoch je nach Art der Intervention und Zielsetzung.
Arzneimittelentwicklung
In der Arzneimittelentwicklung bezieht sich der PoC auf den frühen Nachweis, dass ein therapeutischer Wirkmechanismus beim Menschen relevant ist. Als Wirksamkeitssignale dienen dabei Endpunkte, die eine biologische oder klinische Wirkung plausibel abbilden. Dazu zählen beispielsweise Veränderungen krankheitsrelevanter Biomarker, Effekte auf geeignete Surrogatparameter oder erste Hinweise auf eine Symptomverbesserung oder funktionelle Veränderung.
Medizinprodukte und Medizintechnik
Bei Medizinprodukten und medizintechnischen Verfahren steht im PoC häufig die funktionelle Eignung eines technischen oder interventionellen Konzepts im Vordergrund. Funktionelle Verbesserungen können sich dabei auf messbare Veränderungen beziehen, etwa eine verbesserte Beweglichkeit nach einer orthopädischen Intervention, eine präzisere Steuerung eines Implantats oder eine zuverlässigere Messung physiologischer Parameter. Patientenrelevante Effekte zeigen sich beispielsweise in einer Reduktion von Beschwerden, einer erleichterten Anwendung oder einer Verbesserung alltagsnaher Funktionen. Ziel ist es zu prüfen, ob das Produkt unter klinischen Bedingungen grundsätzlich geeignet ist, einen nachvollziehbaren medizinischen Nutzen zu erzielen.
Diagnostik und Biomarker
In der Diagnostik und Biomarkerforschung dient der PoC dazu zu prüfen, ob ein diagnostischer Ansatz klinisch aussagekräftig ist. Dies kann unterschiedliche Verfahren umfassen, etwa Blut- oder Gewebeanalysen, bildgebende Verfahren oder molekulare Tests. Im Mittelpunkt steht dabei der Abgleich mit etablierten Referenzmethoden, um zu beurteilen, wie zuverlässig eine Krankheit oder ein Krankheitszustand identifiziert wird. Typische Fragestellungen betreffen die Fähigkeit eines Tests, Erkrankte korrekt zu erkennen und Gesunde nicht fälschlich als krank einzuordnen, also das Verhältnis von falsch-positiven und falsch-negativen Ergebnissen. Der PoC liefert hier erste Hinweise darauf, ob ein diagnostisches Verfahren grundsätzlich klinisch nutzbar ist.
Digitale Gesundheitsanwendungen und neue therapeutische Verfahren
Bei digitalen Gesundheitsanwendungen und neuen therapeutischen Verfahren wird im PoC geprüft, ob ein Ansatz unter realistischen Anwendungsbedingungen einen medizinisch relevanten Effekt zeigt. Dazu zählen beispielsweise Apps, die Patientinnen und Patienten bei Übungen, Verhaltenstraining oder Selbstmanagement unterstützen. Wirksamkeitssignale können sich etwa in einer verbesserten Therapietreue, einer Reduktion von Symptomen oder messbaren funktionellen Verbesserungen zeigen. Der PoC soll hier nachvollziehbar belegen, dass der digitale oder neue therapeutische Ansatz grundsätzlich geeignet ist, einen medizinischen Nutzen zu entfalten.
Über alle genannten Anwendungsbereiche hinweg berücksichtigt der PoC neben dem medizinischen oder funktionellen Nutzen häufig auch eine erste Einschätzung der praktischen Umsetzbarkeit im klinischen Alltag. Dabei geht es nicht um eine abschließende Optimierung von Abläufen, sondern um die grundsätzliche Frage, ob ein Ansatz realistisch angewendet werden kann. Aspekte wie zusätzlicher Zeitaufwand, technische Komplexität oder die Integration in bestehende Versorgungsprozesse fließen implizit in die Bewertung ein und können entscheidend dafür sein, ob ein grundsätzlich wirksames Konzept weiterverfolgt wird.
Formale und methodische Grundprinzipien eines Proof of Concept
Unabhängig vom konkreten Anwendungsbereich lassen sich im medizinischen PoC mehrere wiederkehrende methodische Grundprinzipien identifizieren. Sie dienen dazu, mit begrenztem Aufwand eine belastbare Entscheidungsgrundlage zu schaffen, ohne bereits die Anforderungen späterer zulassungsrelevanter Studien zu erfüllen.
- Fokussierte Fragestellung:
Der PoC konzentriert sich auf einen klar definierten Wirkmechanismus oder Ansatz. Ziel ist es, eine eng umrissene Annahme zu prüfen, statt mehrere Fragestellungen parallel zu verfolgen. - Geeignete Endpunkte:
Eingesetzt werden Endpunkte, die einen frühen Effekt möglichst direkt abbilden. Dabei handelt es sich häufig um biologische, funktionelle oder klinisch motivierte Parameter, die sich unter anderem in frühen Biomarkerveränderungen oder durch PK/PD-Modellierung widerspiegeln können. - Begrenzter Studienumfang:
PoC-Studien arbeiten in der Regel mit kleinen Stichprobengrößen und kurzen Beobachtungszeiträumen. Der Fokus liegt auf Effizienz und Signalbewertung, nicht auf statistischer Absicherung. - Flexible Studiendesigns:
Abhängig von Fragestellung und Kontext kommen unterschiedliche Designs zum Einsatz. Randomisierte oder kontrollierte Ansätze sind möglich, aber nicht zwingend erforderlich. - Signalorientierte Auswertung:
Obwohl eine konkrete Hypothese geprüft wird, steht meist die Bewertung von Richtung, Größe und Konsistenz eines Effekts im Vordergrund. Ergebnisse werden als Hinweis interpretiert, nicht als abschließender Wirksamkeitsnachweis. - Entscheidungsorientierung:
Methodik und Auswertung sind darauf ausgerichtet, eine fundierte Go- oder No-Go-Entscheidung für die weitere Entwicklung zu ermöglichen.
Diese Prinzipien verdeutlichen, dass der PoC weniger als formaler Wirksamkeitstest zu verstehen ist, sondern als methodisch strukturierter Entscheidungspunkt innerhalb der medizinischen Entwicklung.
Fazit
Der PoC beschreibt im medizinischen Kontext keinen eigenständigen Studientyp, sondern eine inhaltliche Zielsetzung innerhalb der klinischen Entwicklung. Er dient dazu, frühzeitig zu prüfen, ob ein medizinischer Ansatz beim Menschen einen relevanten Effekt zeigt und damit eine tragfähige Grundlage für die weitere Entwicklung bietet. Typischerweise wird dieses Ziel im Rahmen früher Phase-II-Studien, häufig als Phase IIa bezeichnet, verfolgt.
Unabhängig vom konkreten Anwendungsbereich verfolgt der PoC stets denselben Zweck. Er schafft eine fundierte Entscheidungsgrundlage, bevor umfangreichere Studien oder weiterführende Entwicklungsprogramme gestartet werden. Dabei steht nicht der formale Wirksamkeitsnachweis im Vordergrund, sondern die Identifikation belastbarer Signale, die eine Fortsetzung rechtfertigen oder begründet infrage stellen.
In der Praxis zeigt sich, dass der Aussagewert eines PoC weniger von der Anzahl der erhobenen Daten abhängt als von der klaren methodischen Ausrichtung. Insbesondere die Auswahl geeigneter Endpunkte, die Einordnung der Ergebnisse und die Ableitung einer belastbaren Entwicklungsentscheidung erfordern Erfahrung. Eine frühzeitige methodische Begleitung kann dabei helfen, Fehlschlüsse zu vermeiden und Ressourcen gezielt einzusetzen.
Weiterführende Literatur:
Grill, J.D., Tam, S., Thai, G., Vides, B., Pierce, A.L., Green, K., et al. (2025). Phase 2a proof-of-concept double-blind, randomized, placebo-controlled trial of nicotinamide in early Alzheimer disease. Neurology, 104(1), e210152. https://doi.org/10.1212/WNL.0000000000210152
Karlsson, K. E., Vong, C., Bergstrand, M., Jonsson, E. N., & Karlsson, M. O. (2013). Comparisons of analysis methods for proof-of-concept trials. CPT: Pharmacometrics & Systems Pharmacology, 2(1), e23. https://doi.org/10.1038/psp.2012.24